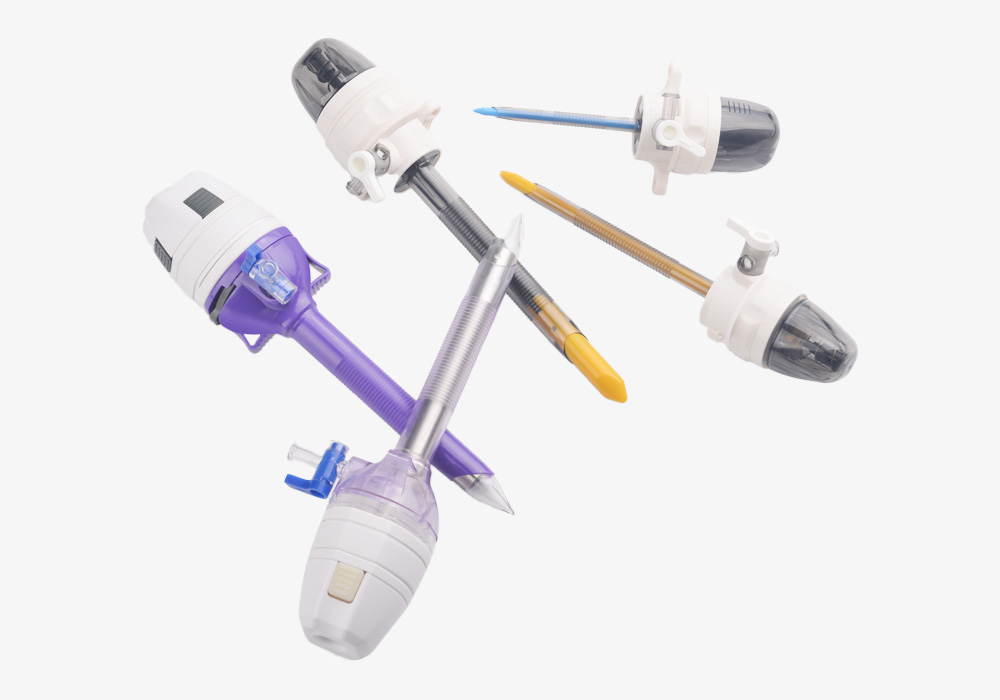
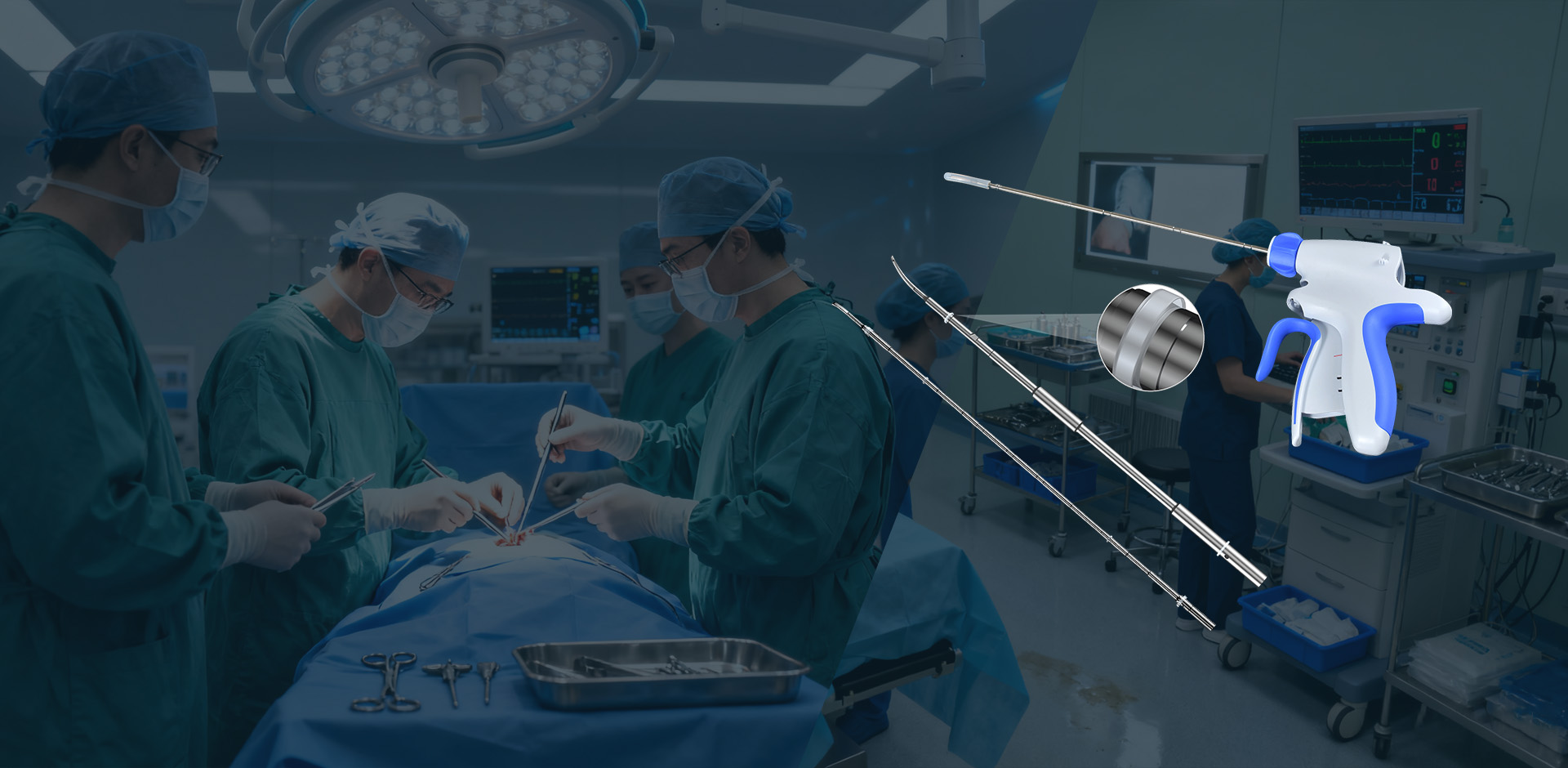
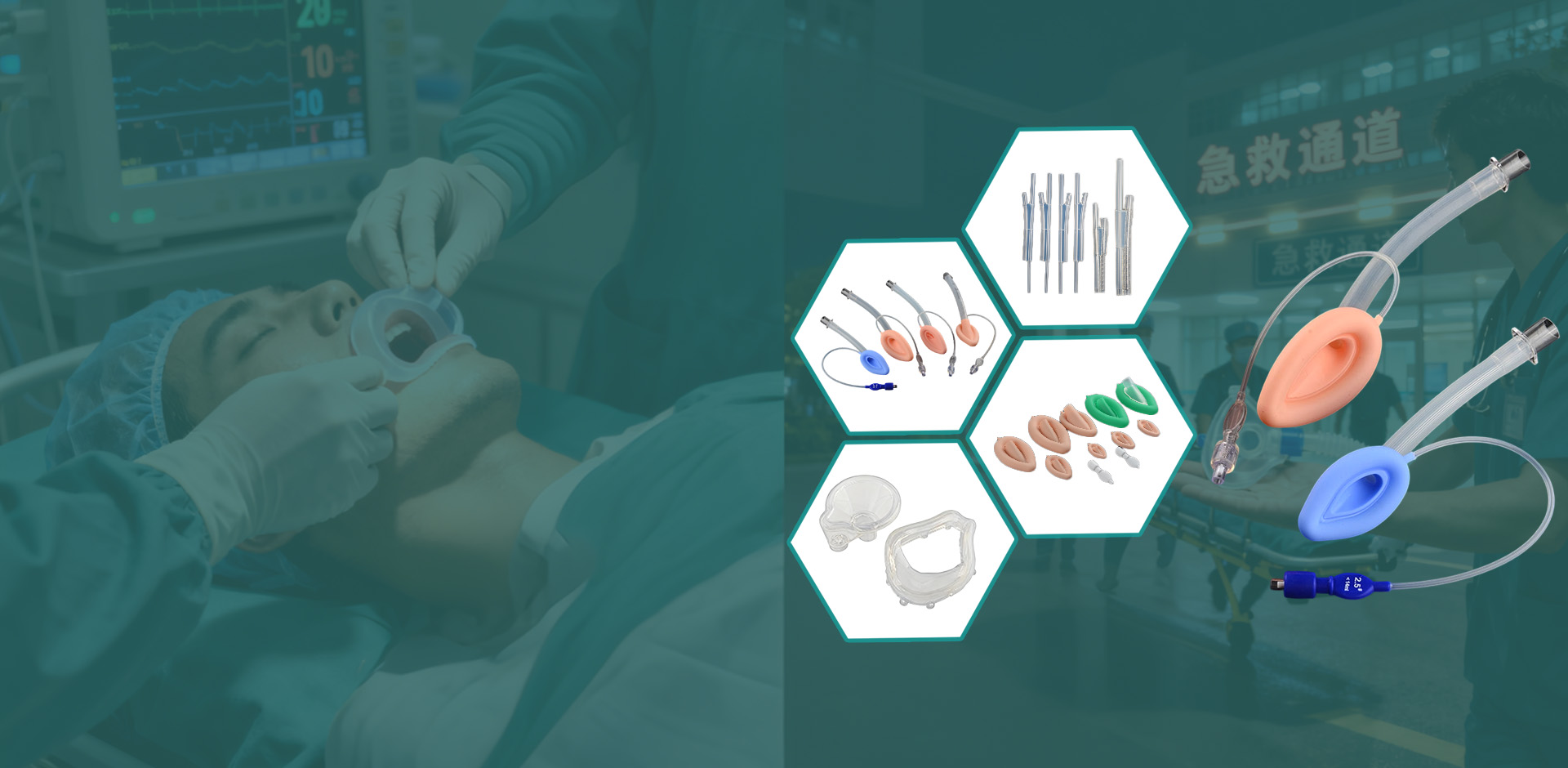
医疗产品的灭菌质量直接关系到患者诊疗安全,是预防交叉感染、保障医疗操作合规性的核心环节。不同材质、用途的医疗产品需适配差异化灭菌方案,需严格遵循国家《医疗器械灭菌 确认和常规控制要求》(GB/T 19633)等标准,确保灭菌效果达到 “无菌保证水平(SAL)不低于 10⁻⁶”,即百万件灭菌产品中微生物存活概率不超过 1 件。目前主流灭菌方法主要分为物理灭菌、化学灭菌两大类,各有适用场景与操作要点。
一、物理灭菌:高效无残留,适配多数耐温医疗产品
物理灭菌通过高温、辐射、压力等物理手段杀灭微生物,因无化学残留、灭菌效果稳定,成为手术器械、植入物等核心医疗产品的首选方案。
高压蒸汽灭菌(湿热灭菌)
作为应用广泛的灭菌方式,适用于耐高温、耐潮湿的医疗产品,如不锈钢手术器械、玻璃器皿、医用硅橡胶制品(如重复使用穿刺器阻气阀)。其原理是利用 121℃(0.1MPa)饱和蒸汽或 134℃(0.2MPa)脉动真空蒸汽,通过热传导破坏微生物蛋白质结构。操作中需注意:
灭菌物品需彻底干燥,避免潮湿导致金属器械锈蚀;腔镜类器械需使用专用灭菌盒,确保蒸汽穿透;灭菌后需在 10-24 小时内使用,超过有效期需重新灭菌。干热灭菌
适用于不耐潮湿但耐高温的产品,如粉末状药品、油脂类敷料、玻璃注射器等。通过 160-180℃干热空气持续 2-4 小时,或 121℃低温干热(适用于热敏性玻璃)持续 12-16 小时实现灭菌。该方法需严格控制温度均匀性,避免局部过热导致产品变形。
辐射灭菌
主要采用 γ 射线、电子束等电离辐射,适用于一次性医疗产品,如注射器、手术衣、口罩、高分子材料制品(如塑料导管)。辐射可穿透包装直接杀灭微生物,且灭菌后无残留、无需通风。需注意:
不适用于含铅、镉等重金属的产品,避免辐射产生有害物质;橡胶类产品需测试辐射耐受性,防止老化变硬。
二、化学灭菌:适配热敏、精密医疗产品
当医疗产品不耐高温、高压时,需采用化学灭菌法,通过化学试剂的杀菌作用实现无菌。
环氧乙烷(EO)灭菌
是精密医疗器械的核心灭菌方式,适用于腔镜、心脏支架、人工晶体、高分子材料制品(如 TPE 材质阻气阀)等热敏、怕潮产品。环氧乙烷通过与微生物蛋白质中的氨基、羟基反应,破坏细胞结构,灭菌温度通常控制在 37-55℃,相对湿度 40%-80%。关键操作要求:
灭菌后需经过 7-14 天通风解析,确保环氧乙烷残留量低于 10μg/g(符合 GB/T 16886.7 标准);易燃易爆,需在专用防爆灭菌柜中进行,且灭菌环境需远离火源。过氧化氢低温等离子体灭菌
适用于不耐环氧乙烷的精密器械,如内镜、牙科手机、电刀笔等。通过将 30%-50% 过氧化氢溶液雾化后,在低温(40-60℃)下形成等离子体,利用活性氧、自由基杀灭微生物,灭菌后无残留、解析时间短(通常 1-2 小时)。需注意:
不适用于多孔、吸水性强的产品(如纱布),避免过氧化氢被吸附导致灭菌不彻底;金属器械需无锈迹,防止等离子体加速腐蚀。过氧乙酸灭菌
适用于环境表面、医疗器械外壳消毒,或不耐高温的小型器械(如喉镜)。通过 0.3%-0.5% 过氧乙酸溶液浸泡、擦拭或喷雾,作用 20-30 分钟实现灭菌。但因腐蚀性较强,需避免长期接触金属、橡胶制品。
三、灭菌效果验证:医疗安全的 “后把关”
无论采用何种灭菌方法,均需通过严格的验证流程确保有效性:
每批次灭菌需放置生物指示物(如含嗜热脂肪杆菌芽孢的菌片),若灭菌后菌片培养阴性,方可判定灭菌合格;定期对灭菌设备进行性能验证,如高压蒸汽灭菌器需每年进行热分布测试,环氧乙烷灭菌柜需每季度测试泄漏率;灭菌记录需至少保存 3 年,便于追溯。
行业专家提醒:灭菌方案需 “一产品一适配”
某医疗器械检测机构灭菌实验室主任指出:“医疗产品灭菌不能‘一刀切’,需结合材质特性、使用场景制定方案 —— 例如重复使用的穿刺器阻气阀,若为全氟橡胶材质可采用高压蒸汽灭菌,若为 TPE 材质则需选择环氧乙烷灭菌。未来随着微创器械向精密化、智能化发展,低温、无残留的灭菌技术(如低温等离子体、紫外光灭菌)将成为研发重点,进一步提升医疗安全水平。”